Os pesquisadores conseguiram ativar o sistema imune, usando exemplares debilitados do patógeno

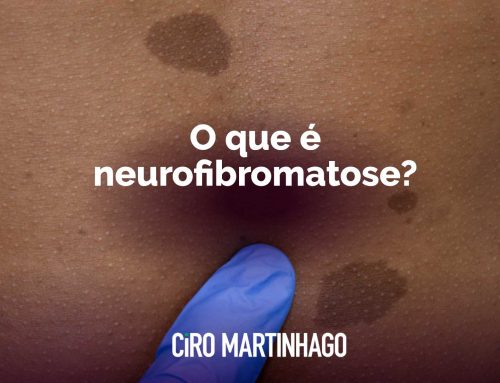
Mosquitos ‘Anopheles’ infectados com o parasita da malária. Foto: CENTER FOR INFECTIOUS DISEASE RESEARCH
A malária é a doença infecciosa que mais mata a cada ano, no mundo, especialmente crianças. Cerca de 300 mil crianças de menos de cinco anos morreram em 2015, devido à malária. Apesar do uso de mosquiteiros, de inseticidas, de remédios, dos milhões de dólares doados para a luta contra a malária, por filantropos como Bill Gates, houve 214 milhões de infectados em 2015, segundo a Organização Mundial da Sáude (OMS). Só o custo de controle da doença superou os 2.400 milhões de euros em 2014.
Mas para vencer a malária falta a arma definitiva: uma vacina que imunize a população exposta. O problema é que o Plasmodium falciparum, a espécie de protozoário que causa a variante mais danosa da doença, é um bicho difícil de combater. Apesar de seu tamanho microscópico, é várias ordens de magnitude mais complexa do que os vírus, tradicionais alvos das vacinas, ou das bactérias.
Além disso, o seu ciclo vital, usando como hospedes mosquitos e humanos em diferentes etapas, complica ainda mais o projeto de uma vacina eficaz. A que mais chegou perto é a RTS,S – desenvolvida pelo laboratório GSK, com participação de investigadores espanhóis da ISGlobal.
Agora, um grupo de investigadores dos Estados Unidos combinou uma das tradições mais antigas da história das vacinas com as modernas ferramentas genéticas, para conseguir uma vacina que, em seus primeiros ensaios, se mostrou segura, logrando um percentual elevado de proteção e de forma duradoura. Eles buscavam atenuar a virulência do parasita para que, sem provocar a malária, pudesse induzir uma resposta do sistema imune. Assim, quando um mosquito infectado com o Plasmodium não modificado picar um ser humano, suas defesas rejeitariam o ataque. Abordagens como esta existem várias entre as mais de 60 candidatas a vacina, segundo a OMS. A diferença neste caso é que, desta vez, os cientistas enfraqueceram o protozoário na sua própria base, na sua genética.
“Identificamos os genes que o parasita necessita para desenvolver-se dentro das células do fígado”, disse o diretor da divisão de ciência translacional do Centro de Investigação de Doenças Infecciosas, Stefan Kappe. Esta organização sem fins lucrativos, com base em Seattle, em colaboração com investigadores do Centro de Investigação Oncológica Fred Hutchinson, criaram uma variedade de Plasmodium falciparum atenuada geneticamente. ” Os três genes suprimidos nos parasitas enfraquecidos são fundamentais para que se estabeleçam nos hepatócitos, protegidos das defesas do hospedeiro “, explica o pesquisador alemão.
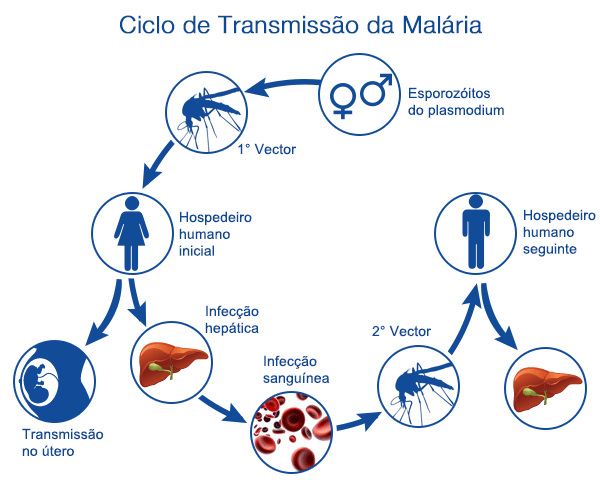
Os investigadores inocularam esses parasitas modificados em uma população de mosquitos Anopheles, o vetor da malária. Ali se desenvolveram até chegar à sua fase infecciosa (esporozoito). Então, uma dezena de voluntários expuseram seus antebraços à picada de 150 a 200 mosquitos. Eles queriam assegurar-se de que o parasita passaria ao humano.
A biologia do Plasmodium mostra que, uma vez na corrente sanguínea de um ser humano, há de chegar até as células hepáticas, onde passará por outra fase vital (merozoito), na qual se multiplica aos milhares. É então que saem do fígado e atacam os glóbulos vermelhos, onde o processo se reinicia. O que esta vacina faz é evitar que os merozoitos saiam das células do fígado.
De acordo com o publicado na revista Science Translational Medicine, a vacina proposta (denominada Pf GAP3KO) se mostrou segura. Os efeitos adversos detectados não foram nada mais do que inchaço, vermelhidão e prurido na zona das picadas.
Sendo um ensaio clínico de fase I, a segurança era o elemento fundamental. Também foi comprovado que nos 10 casos o Plasmodium modificado estimulou o sistema imune. Já nas quimeras (ratos com células hepáticas humanas), os investigadores comprovaram que a vacina as protegia quando foram expostas a cepas do Plasmodium falciparum com seus genes intactos.
Parte do intestino infestada de ‘Plasmodium’. CIDRESEARCH.ORG
“O fundamental nesta fase de investigação é a segurança, que o parasita não reverta à sua característica patogênica”, lembra a chefe do Grupo de Imunologia da Malaria do ISGlobal, de Barcelona, Carlota Dobaño. “Este é o principal marco da pesquisa”, opina. Mas ainda falta muito. Trata-se de uma mostra muito pequena, temos que fazer mais ensaios com maior número de participantes.
Os pesquisadores também terão que encontrar uma forma de simplificar a inoculação do parasita sem depender de centenas de mosquitos, e terão que provar a eficácia da vacina onde mais se sofre de malária, na África Subsaariana.
Todo este caminho já foi percorrido pela vacina STS,S desde que começaram as investigações, há 40 anos. A OMS vai lançar três ensaios de grande escala em 2018. Dependendo dos resultados, recomendará ou não a vacinação em massa. O problema é que, em ensaios recentes, mal ultrapassou os 50% de crianças imunizadas e a proteção é temporária.
“A vacina RTS,S baseia-se em uma única proteína do parasita. A vacina PfGAP3KO parte de todo o parasita com seus 5 mil genes, menos os três que excluímos, por isso promete mais proteção e mais duradoura”, diz Kappe.
Fonte: El País